こんにちは、ボスサラです。そろそろサイエンスに関する記事も書こうかと思います。
以前の会社でやっていた創薬研究を分野外の方にでもわかるように簡単に書いてみました。
炎症と炎症性疾患
みなさん、“炎症性疾患”と聞くとどのようなイメージがあるでしょうか?
例えば、潰瘍性大腸炎、アトピー性皮膚炎、関節性リウマチ、痛風など。これらの疾患は聞いたことがあるかもしれませんね。他にも挙げ始めればキリがありませんが、なんだか怖そうですよね。
では、そもそもこの怖そうな炎症疾患の“炎症“とはなんでしょうか?
Wikipedia(1)によると、
”炎症(えんしょう、英: Inflammation)とは、生体の恒常性を構成する解剖生理学的反応の一つであり、恒常性を正常に維持する非特異的防御機構の一員である。炎症は組織損傷などの異常が生体に生じた際、当該組織と生体全体の相互応答により生じる。”
と書いてあります。少し長いので簡単に表現すると、
“体にとって悪いものを排除して元の状態にする反応”
と言いかえることができます。
例えば、細菌やウイルス(およびそれら感染細胞)の排除。細菌、ウイルスに感染すると体は炎症反応を起こして、元の感染していない状態に戻そうとします。感染症を放っておくと体にとっては悪いことなので、この炎症反応は一種の防御反応に当たります。
そうなんです、炎症は私たちの体にとって必要不可欠な反応なんです。
では、なぜ“炎症”性疾患は怖そうなイメージがあるのでしょうか?炎症の何が問題なのでしょうか??

この答えは炎症のバランスにあります。
炎症は主に炎症性物質(炎症性サイトカイン)というものが免疫細胞に作用することで起こります。適切な量の炎症性サイトカインによって活性化された免疫細胞は適切に異物を排除し、体を元の状態に戻します。
しかし、なんらかの原因で過剰の炎症性サイトカインが免疫細胞に作用すると、免疫細胞が過剰に反応し、結果として暴走してします。暴走した免疫細胞は異物だけでなく正常な細胞にも悪影響を与えてしまいます。
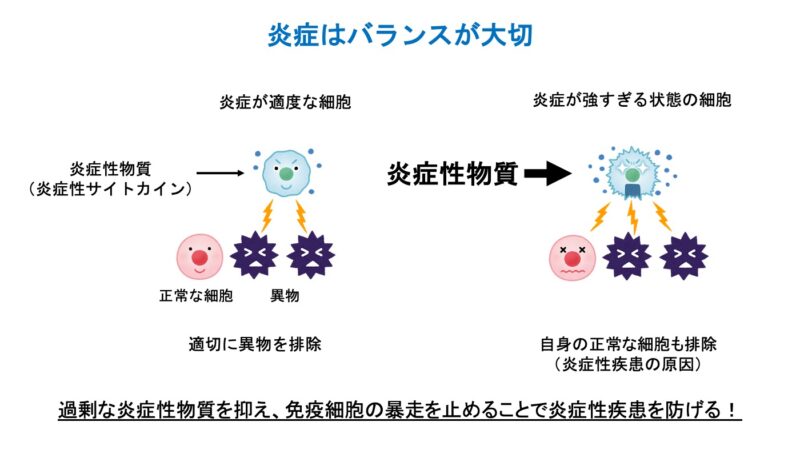
別の見方をすれば、この過剰な炎症性物質を抑え、免疫細胞の暴走を止めることで炎症性疾患を防げるのです。
マクロファージと炎症性の細胞死
では、この“過剰な炎症性物質“はどこから来るのでしょう?私が注目しているのはマクロファージと言われる細胞です。
マクロファージに関しては、アニメ「はたらく細胞」でも紹介されているのでぜひ一度見てみてください。テレビも非常に良くできていて面白いです。はたらく細胞の公式ウェブサイト(2)ではマクロファージの機能として以下のように記載されています。
“細菌などの異物を捕らえて殺し、抗原や免疫情報を見つけ出す。死んだ細胞や細菌を片付ける役割も有している”
しかし、マクロファージが持っている機能はこれだけではありません。私なら以下の文を追加したいです。(はたらく細胞の公式ウェブサイトにもいつか書いて欲しい!)
“自爆して自身の細胞内から炎症性物質(炎症性サイトカイン)を放出し炎症を引き起こす。”
百聞は一見にしかず。顕微鏡下でのマクロファージの役割を動画で見てみましょう。(3)
一つ一つがマクロファージ細胞です。ある刺激を加え、細胞を染色しています。いかにも細胞が自爆して炎症を起こしそうですよね。
この自爆は専門用語でパイロプトーシス (Pyroptosis)とよばれています。ギリシャ語で
”Pyro-”= “炎“
”-ptosis”=”落ちる”(この場合は生きた細胞集団から落ちて細胞が死ぬという意味)
を意味します。
つまり、Pyroptosisとは炎症性の細胞死(細胞が炎のように燃えて死ぬ)を意味します。そしてこのPyroptosisこそが炎症性疾患と深い関係にあるのです。
Pyroptosisの分子メカニズム
それでは、このPyroptosisの分子メカニズムはどうなっているのでしょうか?
下図を見ながら順を追って説明します。
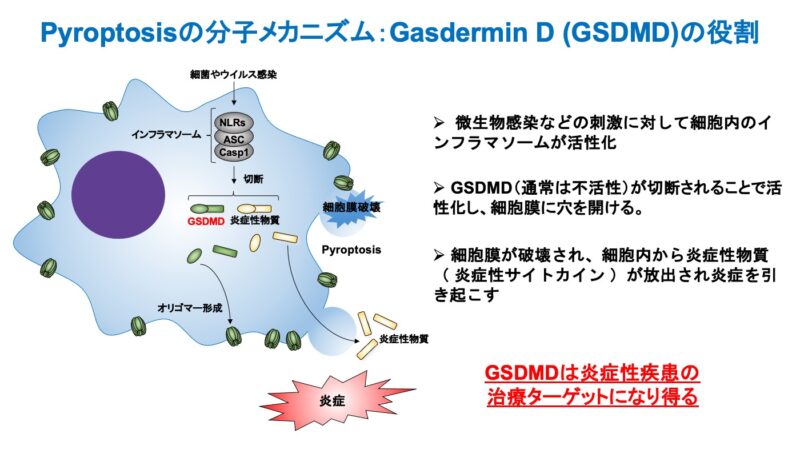
まず、マクロファージに微生物感染(細菌やウイルスの感染)などの刺激に対して細胞内の“インフラマソーム”とよばれる複合体が形成されます。
この複合体が活性化すると、最終的にその構成分子の一つであるCaspase-1 (Casp1)という酵素が活性化します。Casp1は様々な細胞内の分子を切断することが知られているのですが、その中の一つとしてGasdermin D (GSDMD)というものを切断することがわかりました。(4, 5)
GSDMDは通常では不活性化されているのですが、Casp1よって切断されると活性化し、その一部(図の楕円)が集まって(オリゴマー形成)、筒状となることで細胞膜に穴を開けます。イメージすると型抜きクッキーで穴を開ける感じですかね。
穴の開いた細胞膜は破壊されてしまい、細胞内にある炎症性物質(炎症性サイトカイン)が放出されることで炎症を引き起こします。
そして、このGSDMDの活性化が強すぎると炎症が強く引き起こされ、炎症性疾患の原因になる可能性があるのです。
これらを総合して考えると、GSDMDを阻害することで強い炎症を抑えることができ、様々な炎症性疾患を治療することができるかもしれません。GSDMDは炎症性疾患の治療ターゲットになり得るのです!
GSDMDと炎症性疾患
それでは、本当にGSDMDを阻害すれば炎症性疾患の治療ができるのでしょうか?
ここでは家族性地中海熱(Familial Mediterranean Fever:FMF)という炎症性疾患を例に見てみたいと思います。
家族性地中海熱とは発作性におこる発熱と腹部、胸部の疼痛や関節の腫れなどの症状が繰り返される遺伝性の病気です(6)。家族性地中海熱の患者さんは下図のような皮膚の赤い発疹が見られる場合があります(7)。
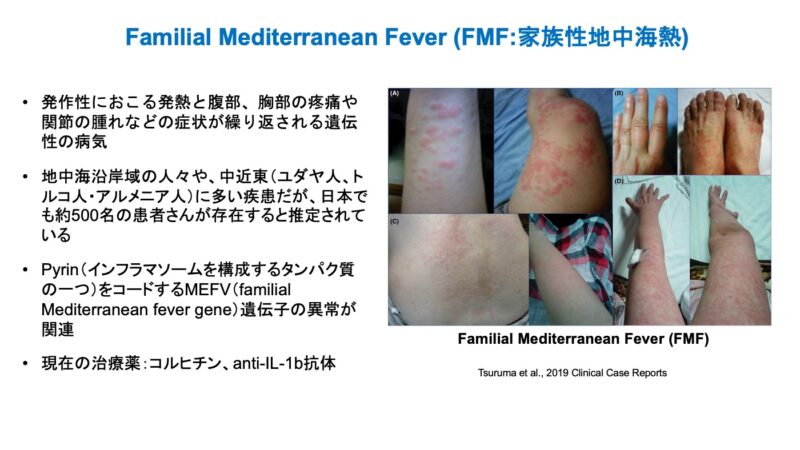
この疾患は希少疾患であまり患者さんがいないことから、一般の人はあまり聞いたことがないかもしれません。(私も研究を始める前まで知りませんでした)
希少疾患とはいえ、患者さんの分布を見ると地中海沿岸域の人々や、中近東(ユダヤ人、トルコ人・アルメニア人)には比較的多い疾患です。日本でも約500名の患者さんが存在すると推定されています。
原因遺伝子に関しては比較的良く研究がされていて、Pyrin(インフラマソームを構成するタンパク質の一つ)をコードするMEFV(familial Mediterranean fever gene)遺伝子の異常が関連すると考えられています。
現在の治療法としては抗炎症作用のある薬としてコルヒチンや抗IL-1β抗体が使用されています。
家族性地中海熱には異常があるヒトのMEFV遺伝子を導入したマウスモデルが存在します。このマウスは正常なマウスと比べ、家族性地中海熱の症状である皮膚の異常が見られ、血中の炎症性サイトカイン(IL-1β)が高い特徴が見られます。
驚いたことに、このマウスからGasdermin Dを欠損させると、皮膚の異常が見られなくなり、高かった炎症性サイトカイン(IL-1β)の値も正常なマウスとほぼ変わらなくなることがわかりました(8)。
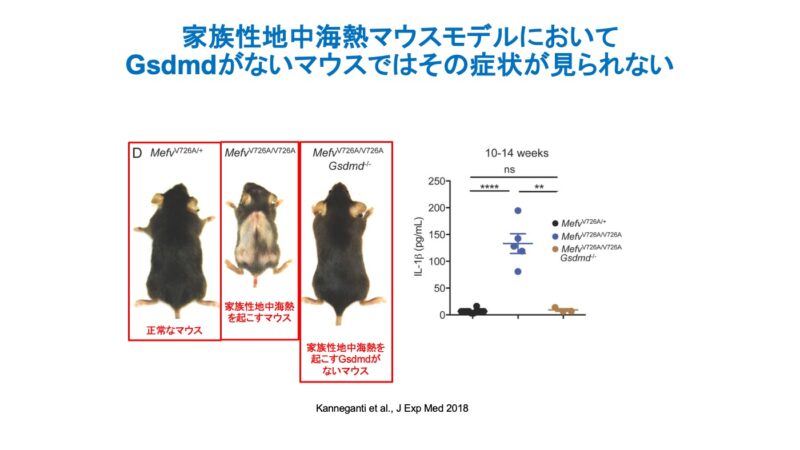
つまり、GSDMDを欠損した状態(≒阻害した状態)では炎症性疾患の症状が抑えられることが示唆されるのです。これはGSDMDが欠損したことによりマクロファージの炎症性細胞死(Pyroptosis)が起こらなくなったためと考えられます。
これらのことからGasdermin Dの阻害剤を作ることができれば、炎症性疾患の治療薬になるかもしれないのです!
最後に
以上、現在私が行なっている創薬研究に関する記事でした。いつかGasdermin Dの阻害剤が作れると信じてチャレンジしていますが、なかなかタフなターゲットです。
今後も免疫、炎症性疾患、細胞死などをキーワードに創薬研究をするので関連するサイエンスの情報を記事にしていきたいと思います。
References
1. 炎症 – Wikipedia:https://ja.wikipedia.org/wiki/%E7%82%8E%E7%97%87
2. TVアニメ「はたらく細胞!!」:https://hataraku-saibou.com/
3. Jorgensen et al. J Exp Med. 2016 Pyroptosis triggers pore-induced intracellular traps (PITs) that capture bacteria and lead to their clearance by efferocytosis
4. Kayagaki et al. Nature 2015 Caspase-11 cleaves gasdermin D for non-canonical inflammasome signalling.
5. Shi et al. Nature 2015 Cleavage of GSDMD by inflammatory caspases determines pyroptotic cell death.
6. 家族性地中海熱(指定難病266) – 難病情報センター:https://www.nanbyou.or.jp/entry/4447
7. Tsuruma et al. Clin Case Rep. 2019 An adult case of atypical familial Mediterranean fever (pyrin-associated autoinflammatory disease) similar to adult-onset Still’s disease.
8. Kanneganti et al. J Exp Med. 2018 GSDMD is critical for autoinflammatory pathology in a mouse model of Familial Mediterranean Fever.


